1) la Commissione Europea approva isatuximab
L’approvazione europea si basa sui dati dello studio clinico randomizzato di fase 3 ICARIA-MM, il primo ad aver valutato un anticorpo anti-CD38 in combinazione con pomalidomide e desametasone (pom-dex)
• Isatuximab in combinazione con pom-dex ha ridotto significativamente il rischio di progressione di malattia o di morte, rispetto al solo trattamento con pom-dex
2) STUDIO DI FASE 3 IKEMA
La terapia di associazione con isatuximab ha dimostrato una sopravvivenza libera da progressione superiore e una profondità di risposta clinicamente significativa in pazienti con mieloma multiplo recidivato
• L’aggiunta di isatuximab a carfilzomib e desametasone (terapia di associazione con isatuximab) ha ridotto significativamente il rischio di progressione della malattia o morte, rispetto allo standard di cura con i soli carfilzomib e desametasone (Kd)
• Con la terapia di associazione con isatuximab si è ottenuta una profondità di risposta importante, con mieloma multiplo (MM) non rilevabile in una percentuale significativa dei pazienti con MM recidivato (MRD-negativi a una sensibilità di 10-5)
• I risultati della prima analisi ad interim pianificata dello studio di fase 3 IKEMA sono stati accettati come presentazione late-breaking al 25° Congresso EHA che si terrà in modalità virtuale
• Il mieloma multiplo è la seconda neoplasia ematologica per diffusione, con circa 40.000 nuovi casi ogni anno in Europa
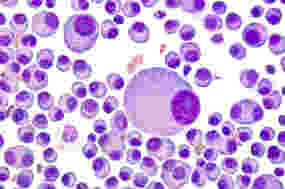
Isatuximab è un anticorpo monoclonale (mAb) che si lega a uno specifico epitopo del recettore CD38 sulle cellule di mieloma multiplo.
“L’approvazione di isatuximab da parte della Commissione Europea aggiunge un’ importante opzione di trattamento e potrebbe definire un nuovo standard di cura per quei pazienti europei con mieloma che necessitano di nuovi trattamenti efficaci perché la malattia si è ripresentata oppure sono diventati refrattari a precedenti terapie,” commenta John Reed, Responsabile della Ricerca e Sviluppo di Sanofi a livello globale. “Isatuximab in combinazione con pom-dex ha dimostrato una mediana di sopravvivenza libera da malattia superiore rispetto al solo pom-dex, in pazienti che hanno già fallito almeno due precedenti terapie.”
L’autorizzazione alla commercializzazione della Commissione Europea per isatuximab si applica ai 27 Stati membri dell’Unione Europea, più Regno Unito, Islanda, Lichtenstein e Norvegia.
Il profilo di efficacia e sicurezza di isatuximab in pazienti difficili da trattare
Nello studio di fase 3 ICARIA-MM, con l’aggiunta di isatuximab a pom-dex (terapia di associazione con isatuximab) si è ottenuto un miglioramento statisticamente significativo della sopravvivenza libera da progressione(PFS). La terapia di associazione con isatuximab ha anche dimostrato un tasso di risposta complessivo significativamente maggiore rispetto al solo trattamento pom-dex..
In ulteriori analisi, la terapia di associazione con isatuximab ha dimostrato, rispetto al solo pom-dex, un beneficio terapeutico consistente in alcuni sottogruppi selezionati di pazienti, rappresentativi della pratica clinica del mondo reale, compresi i pazienti con citogenetica ad alto rischio, quelli di età pari o superiore a 75 anni, i pazienti con insufficienza renale e i pazienti che erano refrattari alla lenalidomide.
“Ogni volta che il mieloma multiplo recidiva oppure diventa resistente al trattamento, diventa sempre più difficile da trattare e la prognosi per i pazienti peggiora significativamente,” commenta Sara Bringhen, A.O.U. Città della Salute e della Scienza di Torino e principal investigator degli studi clinici con isatuximab in Italia. “Nello studio clinico ICARIA-MM, che in Italia ha coinvolto 8 centri e 24 pazienti, la terapia di associazione con isatuximab ha dimostrato un beneficio terapeutico consistente in tutti sottogruppi di pazienti con mieloma multiplo recidivato e refrattario. Isatuximab rappresenta, quindi, una nuova importante opzione di trattamento e ha il potenziale per diventare il nuovo standard di cura per i pazienti con mieloma multiplo recidivato e refrattario"
STUDIO DI FASE 3 IKEMA
L’aggiunta di isatuximab alla terapia con carfilzomib e desametasone (terapia di associazione con isatuximab) ha ridotto significativamente il rischio di progressione della malattia o morte rispetto allo standard di trattamento con carfilzomib e desametasone (Kd) in pazienti con mieloma multiplo (MM) recidivato. Rispetto al solo Kd, la terapia di associazione con isatuximab ha dimostrato un beneficio terapeutico coerente tra più sottogruppi.
Questi risultati dello studio di fase 3 IKEMA fanno seguito all’annuncio preliminare dello scorso 12 maggio relativo al raggiungimento dell’endpoint primario dello studio nel corso dell’analisi ad interim pre-pianificata. I risultati ad interim saranno presentati durante la sessione late-breaking del Congresso virtuale della European Hematology Association (EHA25) il prossimo 14 giugno e costituiranno la base dei dossier da sottomettere alle agenzie regolatorie nel corso di quest’anno.
“Nello studio di fase 3 IKEMA, l’aggiunta di isatuximab a carfilzomib e desametasone ha ridotto significativamente il rischio di progressione di malattia o morte rispetto al solo trattamento con carfilzomib e desametasone,” dichiara Sara Bringhen, A.O.U. Città della Salute e della Scienza di Torino e principal investigator degli studi clinici per isatuximab in Italia. “I risultati di questo studio clinico – che ha coinvolto anche alcuni centri e pazienti italiani – suggeriscono il potenziale di isatuximab di diventare un nuovo standard di trattamento del mieloma multiplo recidivato.”
La sicurezza e la tollerabilità di isatuximab osservate in questo studio sono coerenti con il profilo di sicurezza di isatuximab osservato in altri studi clinici, senza la rilevazione di alcun nuovo segnale di sicurezza.
“Questo è il secondo studio clinico di fase 3 che dimostra la superiorità della terapia di associazione con isatuximab rispetto allo standard di trattamento, che si aggiunge alla mole di evidenze che dimostrano come il nostro anticorpo monoclonale anti-CD38 abbia il potenziale per fare una differenza significativa per i pazienti”, commenta John Reed, Responsabile della Ricerca e Sviluppo di Sanofi a livello globale. “Siamo convinti che isatuximab abbia il potenziale per diventare l’anti-CD38 d’elezione nel trattamento del mieloma multiplo. Attendiamo di vedere i risultati dei prossimi studi clinici per comprendere l’impatto di isatuximab in fasi più precoci di malattia.”
Fonte: Ufficio Stampa Sanofi
 Feed RSS
Feed RSS
